Personalisierte Lungendiagnostik
Die AG Personalisierte Lungendiagnostik ist eine interdisziplinäre Arbeitsgruppe, die eng mit den verschiedenen Fachbereichen des Westdeutschen Lungenzentrums (Universitätsmedizin Essen, Ruhrlandklinik) und dem Institut für Künstliche Intelligenz in der Medizin (IKIM, Forschungsgruppe: Data Integration and AI in Radiology) zusammenarbeitet.
Der Fokus liegt einerseits auf der Implementierung der Lungenkrebsfrüherkennung mittels Niedrigdosis-Computertomographie und andererseits auf der Nutzung neuer Technologien aus der Informationstechnologie / Data Science zur Lösung bestehender Fragestellungen in der Thoraxradiologie.
Forschungsschwerpunkte
Lungenkrebsfrüherkennung in Deutschland
Lungenkrebs ist in Deutschland eine der häufigsten Krebserkrankungen und Todesursachen. Im Frühstadium treten häufig keine Beschwerden auf, so dass Lungenkrebs oft erst im fortgeschrittenen oder metastasierten Stadium diagnostiziert wird. Eine Früherkennung verbessert jedoch die Behandlungsmöglichkeiten und damit die Prognose für die Betroffenen.
Der Nutzen eines ganzheitlichen und effektiven Lungenkrebsfrüherkennungsprogramms mit Niedrigdosis-Computertomographie für Risikopatienten zur Senkung der Lungenkrebsmortalität konnte bereits in mehreren nationalen und internationalen Studien gezeigt werden. In der aktuellen S3-Leitlinie zur Prävention, Diagnostik, Therapie und Nachsorge des Lungenkarzinoms wird bereits eine jährliche Niedrigdosis-Computertomographie für Risikopatienten empfohlen.
Bei der Umsetzung eines Lungenkrebs-Früherkennungsprogramms gibt es jedoch Bedenken hinsichtlich einer optimalen Rekrutierungsstrategie und einer ökonomischen Umsetzung. Die Machbarkeit der Umsetzung im Detail wird derzeit in einem von der EU geförderten Projekt „4-In The Lung Run“ untersucht, an dem auch wir als Standort Essen beteiligt sind.
Darüber hinaus entwickeln und validieren wir neue Bildverarbeitungs- und Analysemethoden, um eine höhere Sensitivität und Spezifität bei der Erkennung von Lungenkrebs zu erreichen und die Strahlenbelastung zu reduzieren.
„SMART Pneumology“ – Mit künstlicher Intelligenz (KI) zum Lungenrundherd
In enger Zusammenarbeit mit der interventionellen Pneumologie der Ruhrlandklinik Essen haben wir als weltweit erste das KI-System (Archimedes™) auf einem Photon-Counting-CT erfolgreich implementiert, um eine präzise Navigation zur Abklärung von Lungenrundherden zu ermöglichen. Mit Hilfe spezieller CT-Bilder des Patienten kann das System den genauen Weg zum Lungenherd über die Atemwege und durch das Lungengewebe planen. Während der Untersuchung wird der Weg zum Lungenherd als Augmented Reality in das Bronchoskopie- und Durchleuchtungsbild eingeblendet, so dass das Ziel millimetergenau angesteuert und die Gewebeproben unter Durchleuchtungskontrolle gezielt entnommen werden können.
Das NAEOTOM Alpha® ermöglicht eine höhere spektrale Auflösung und Bildqualität durch den Einsatz der Quantum HD-Auflösung mit einer Schichtdicke von 0,2 mm und einem verbesserten Kontrast-Rausch-Verhältnis. Für die bronchoskopische Abklärung von Lungenherden erhofft man sich dadurch eine bessere Erreichbarkeit peripherer Herde bei gleichzeitig reduzierter Strahlenbelastung für die PatientInnen.

CT-basierte vollautomatische Body Composition and Body Organ Analysis (BCA/BOA) in der Thoraxradiologie
In Zusammenarbeit mit dem Institut für Künstliche Intelligenz in der Medizin (IKIM, Forschungsgruppe: Data Integration and AI in Radiology) wurde eine Deep-Learning-Netzwerkarchitektur entwickelt, die auf einer mehrstufigen 3D U-Net-Architekturvariante basiert und eine vollautomatisierte Segmentierung von Gewebestrukturen/-komponenten aus CT-Scans ermöglicht.
Der am häufigsten verwendete Biomarker zur Abbildung der Körperzusammensetzung von Menschen ist bisher der Body-Mass-Index (BMI). Trotz seiner weiten Verbreitung hat der BMI erhebliche Einschränkungen, da er die Verteilung spezifischer Körpergewebe (z.B. Fett, Muskel oder Knochen) nicht berücksichtigt. Die an der Universitätsmedizin Essen entwickelte CT-basierte vollautomatische Körper- und Organzusammensetzungsanalyse (BCA/BOA) liefert zusätzliche Informationen und ermöglicht z.B. die Überwachung von Risikofaktoren wie Sarcopenie oder Adipositas in CT-Scans. Wir konzentrieren uns bei der Anwendung auf die Analyse verschiedener chronischer und maligner Lungenerkrankungen.
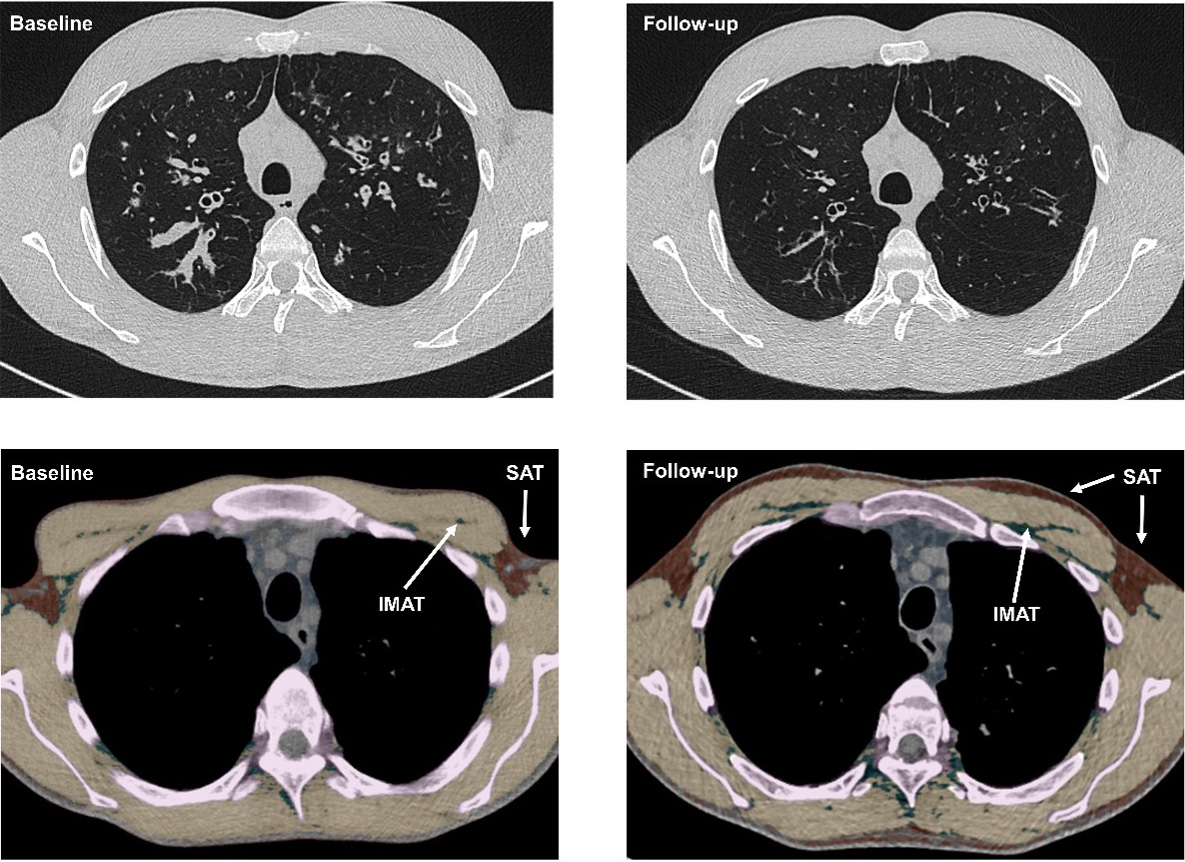
Im folgenden Beispiel wurde die Körperzusammensetzung von Mukoviszidose PatientInnen, die mit einer Cystic Fibrosis Transmembrane Conductance Regulator (CFTR) Therapie behandelt wurden, mittels Thorax-CT untersucht. In erster Linie führte die CFTR Modulator Therapie zu einer Zunahme des Fettgewebes (total adipose tissue +46%; SAT, subcutaneous adipose tissue +50%; IMAT, intra- and intermuscular adipose tissue +34.62%). Die Ergebnisse unserer Studie haben Auswirkungen auf die Empfehlungen für das zukünftige Ernährungsmanagement von Mukoviszidose PatientInnen.
Kooperationen
Extern
- Dr. med. Daniel Majorski (Lungenzentrum Köln-Merheim)
- Prof. Dr. med. Mark Oliver Wielpütz (Universitätsklinikum Heidelberg)
Intern
- Univ.-Prof. Dr. med. Felix Nensa, Hybride Arbeitsgruppe (Radiologie/KI) / Teil des Instituts für künstliche Intelligenz in der Medizin
- Priv.-Doz. Dr. med. Johannes Haubold, AG Klinische KI-Integration
- Prof. Dr. med. Hubertus Hautzel, Klinik für Nuklearmedizin
- Dr. med. David Kersting, M.Sc., Klinik für Nuklearmedizin
- PD Dr. med. Nika Guberina, Klinik für Strahlentherapie
- Univ.-Prof. Dr. med. Christian Taube, Klinik für Pneumologie (Ruhrlandklinik Essen)
- Prof. Dr. med. Kaid Darwiche, Interventionelle Bronchologie (Ruhrlandklinik Essen)
- Dr. med. Dr. Sivagurunathan Sutharsan, Klinik für Pneumologie (Ruhrlandklinik Essen)
- Dr. med. Matthias Welsner, Klinik für Pneumologie (Ruhrlandklinik Essen)
- Dr. med. Dirk Westhölter, Klinik für Pneumologie (Ruhrlandklinik Essen)
- Prof. Dr. med. Christoph Schöbel, Klinik für Pneumologie (Ruhrlandklinik Essen)
- Dr. med. Johannes Wienker, Interventionelle Bronchologie (Ruhrlandklinik Essen)
- Dr. med. Julia Wälscher, Klinik für Pneumologie (Ruhrlandklinik Essen)
- Priv.-Doz. Dr. med. Filiz Özkan, Interventionelle Bronchologie (Ruhrlandklinik Essen)
- Faustina Funke, Interventionelle Bronchologie (Ruhrlandklinik Essen)
- Priv.-Doz. Dr. med. Florian Stehling, Kinderpneumologie
Team

Priv.-Doz. Dr. med.
Marcel Opitz

Dr. med.
Marko Frings, M.Sc.

Abdullatif Kocak

Halil Ibrahim Tazeoglu
Doktoranden
Abdullatif Kocak, Christin Mousa, Halil Tazeoglu, Celina Zenk
Westhölter, D., Haubold, J., Welsner, M., Salhöfer, L., Wienker, J., Sutharsan, S., Straßburg, S., Taube, C., Umutlu, L., Schaarschmidt, B. M., Koitka, S., Zensen, S., Forsting, M., Nensa, F., Hosch, R. & Opitz, M. Elexacaftor/tezacaftor/ivacaftor influences body composition in adults with cystic fibrosis: a fully automated CT-based analysis. Sci Rep 14, 9465, doi:10.1038/s41598-024-59622-2 (2024).
Wienker, J., Darwiche, K., Rüsche, N., Büscher, E., Karpf-Wissel, R., Winantea, J., Özkan, F., Westhölter, D., Taube, C., Kersting, D., Hautzel, H., Salhöfer, L., Hosch, R., Nensa, F., Forsting, M., Schaarschmidt, B. M., Zensen, S., Theysohn, J., Umutlu, L., Haubold, J. & Opitz, M. Body composition impacts outcome of bronchoscopic lung volume reduction in patients with severe emphysema: a fully automated CT-based analysis. Sci Rep 14, 8718, doi:10.1038/s41598-024-58628-0 (2024).
Meetschen, M., Sandach, P., Darwiche, K., Theegarten, D., Moter, A., Schaarschmidt, B. M., Herrmann, K., Fendler, W. P., Hautzel, H. & Opitz, M. in Eur J Nucl Med Mol Imaging 1-3 (2023).
Hlouschek, J., König, B., Bos, D., Santiago, A., Zensen, S., Haubold, J., Pöttgen, C., Herz, A., Opitz, M., Wetter, A., Guberina, M., Stuschke, M., Zylka, W., Kühl, H. & Guberina, N. Experimental Examination of Conventional, Semi-Automatic, and Automatic Volumetry Tools for Segmentation of Pulmonary Nodules in a Phantom Study. Diagnostics (Basel) 14, doi:10.3390/diagnostics14010028 (2023).
